Capa de Ozono: A recuperarse de a poco.
El ozono (O3) se encuentra mayoritariamente entre 10 y 50 kilómetros de altura, en la estratósfera. Esta capa es conocida como la capa de ozono. Este ozono de alta altura es muy beneficioso, ya que absorve la radiación UV. Sin la existencia de esta capa la vida fuera de los océanos sería prácticamente imposible. Pero también se encuentra ozono en menor medida entre la superficie terrestre y los 10 kilómetros de altura. Este ozono es el llamado ozono de nivel de suelo, en tanto, no cumple ningún papel beneficioso. Más aún, debido a ser muy tóxico es un grave problema para las grandes urbes que lo producen. Un ejemplo de esto es Santiago de Chile.
La producción de ozono ocurre principalmente a través de la fotólisis de oxígeno molecular. Existe una disociación molecular de oxígeno (O2) en átomos simples de este (O). Este proceso es producido por la radiación de onda corta de luz ultravioleta (UV). Luego, estos átomos simples (O) al unirse con una molécula de oxígeno (O2) forman ozono (O3).
El ozono es un gas muy fundamental, pero también extremadamente raro en la atmósfera, ya que existe una relación de 3 moléculas de ozono por cada 10 millones de moléculas de aire. Este gas se mide en Unidades Dobson. Mil Unidades Dobson equivalen a una columna uniforme de ozono de un centímetro de espesor en condiciones normales de presión (1atm o nivel del mar) y temperatura (273K o cero grados Celsius).
Hay que precisar que siempre hay que tener en cuenta la época y el lugar para decidir si los niveles de ozono que se están midiendo corresponden a niveles altos o bajos. La capa de ozono varía según época y lugar geográfico en que uno se encuentra.
En el polo Norte las temperaturas estratosféricas son más elevadas, por lo que no se forman tantas nubes y la destrucción de ozono es mucho menor.
El pasado 16 de Septiembre, la Organización de las Naciones Unidas celebro el Día Internacional para la Preservación de la Capa de Ozono y concienciar así a la comunidad internacional de la necesidad de protegerla. Los expertos anunciaron un agravamiento del problema durante este año y aseguraron que nunca en la historia del planeta la capa de ozono había sido tan delgada y con tantos agujeros.
En 1985 se detectó que sobre la Antártida había desaparecido la capa de ozono que protege a la Tierra de los rayos ultravioleta del sol. Los científicos demostraron que los causantes del problema eran una serie de gases artificiales que se comían las partículas de ozono. -utilizados en aerosoles, frigoríficos y refrigerantes- empezaron a ser regulados a nivel internacional aunque, a la vista de los resultados, de una manera bastante insuficiente.
Los primeros datos sobre el comienzo de un deterioro de la capa de ozono se remontan al año 1982, cuando los valores sobre la columna de ozono obtenidos por la estación japonesa Syowa en la Antártida (69S, 39E) se dan a conocer. Los niveles de la columna de ozono registrados desde el año 1964 indicaban que a partir del año 1975 esta presentaba un claro deterioro.
Resultados similares se publicaron posteriormente en otras estaciones ubicadas en el continente Antártico, coincidiendo en todas ellas que el deterioro comenzó en la década de los 70. Este daño de la capa de ozono registrado en la Antártida aparecía en todas las estaciones al comienzo de la primavera Austral y tenía en aquellos años una corta duración y una rápida recuperación. Todo esto llevó a una alarma en la comunidad mundial, pues sus concecuencias, de no frenarse el proceso, podían ser de un alcance importante.
Años después de la publicación del deterioro de la capa de ozono sobre el continente Antártico, tuvo lugar un hecho fundamental para el entendimiento posterior del fenómeno denominado Agujero de Ozono. El científico inglés J. Lovelock tenía el proyecto de investigar la dinámica de la alta atmósfera, para lo cual buscó compuestos químicos que fueran enviados periódicamente a la atmósfera y que tuvieran una larga vida antes de descomponerse. Siguiendo la pista de estos elementos podría conocerse cuáles eran las corrientes que los llevaron del lugar de uso hasta el punto de destino.
Había entonces que elegir esos compuestos que servirían de marcadores, tenían que ser consumidos en cierta cantidad y tener una larga vida, para así poder ser seguidos durante su posible largo recorrido. Lovelock encontró sus marcadores ideales en los Clorofluorocarbonos (CFCs), compuestos sintéticos sobre los años 20 y que eran, y son hoy en día, utilizados en aplicaciones muy comunes como pulverizadores y disolventes, así como por las industrias del frío y de los aislantes térmicos. Con sorpresa encontró, siguiendo la huella de estos compuestos una inesperada y alta concentración de los mismos en el continente Antártico.
La alta estabilidad de los compuestos CFCs aseguraba en principio un papel inofensivo de los mismos, por ello se han ocupado en tantas aplicaciones. Sin embargo en 1972 Molina y Rowland llamaron la atención de que el desprendimiento de cloro de estos compuestos al ser expuestos a la radiacióEl incremento de la radiación UV-B:
La forma por la cual se destruye el ozono es bastante sencilla. La radiación UV arranca el cloro de una molécula de clorofluorocarbono (CFC). Este átomo de cloro, al combinarse con una molécula de ozono la destruye, para luego combinarse con otras moléculas de ozono y eliminarlas. El proceso es altamente dañino, ya que en promedio un átomo de cloro es capaz de destruir hasta 100.000 moléculas de ozono. Este proceso se detiene finalmente cuando este átomo de cloro se mezcla con algún compuesto químico que lo neutraliza.
Aunque las moléculas de CFC son varias veces más pesadas que el aire, miles de mediciones hechas mediante globos, aviones y satélites han demostrado que los CFCs se encuentran en la atmósfera hoy en día. Hay que considerar que la atmósfera no está quieta, sino que los vientos la revuelven constantemente antes que las partículas pesadas puedan "decantar" y llegar a la superficie. Particularmente los CFCs que son insolubles en el agua y muy estables en la baja atmósfera (debajo de los 10 Km.) llegan a la alta atmósfera en donde se encuentra el ozono.
Existen muchos compuestos naturales sobre la superficie terrestre que contienen cloro, pero ellos son solubles en agua, por lo que no pueden alcanzar la estratósfera. Grandes cantidades de cloro (en forma de cloruro de sodio) son evaporadas de los océanos, pero son solubles en agua por lo que son atrapados por las nubes y vuelven a bajar en gotas de agua, nieve o hielo.
Otra fuente de de cloro es el de las piscinas, pero este cloro también es soluble en agua. El cloruro de hidrógeno, producto de las las erupciones volcánicas es un claro ejemplo de un contaminante natural, pero este cloro es convertido en ácido clorhídrico, el cual es soluble en agua por lo que no alcanza la estratósfera.
En cambio, halocarbonos hechos por el hombre, como los CFCs, tetracloruro de carbono (CCI4) y metil cloroformo (CH·CCI3) no son solubles en el agua, por lo que no caen con la lluvia o nieve y alcanzan la estratósfera.
Es un hecho que los contaminantes, como los CFC se producen mayoritariamente en el hemisferio norte. El 90% es liberado en Europa, Rusia, Japón y EEUU. Los CFC suben luego hacia la estratósfera en las latitudes tropicales debido a los vientos. En seguida estos contaminantes son trasladados mediante vientos hacia ambos polos. Así la estratósfera contiene aproximadamente un contenido homogéneo de cloro sobre todas las latitudes. Pero ambos polos tienen una meteorología muy
diferente debido a su distinta superficie terrestre.
El polo Sur tiene grandes extensiones de tierra, las cuales están rodeadas de mar. Estas condiciones producen bajas temperaturas en la estratósfera, lo que crea nubes polares estratosféricas. Finalmente estas nubes crean un ambiente químico propicio para la destrucción de ozono en la época de Primavera Austral, que se extiende entre septiembre hasta diciembre cada año.
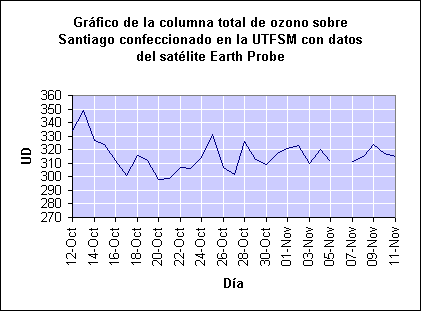
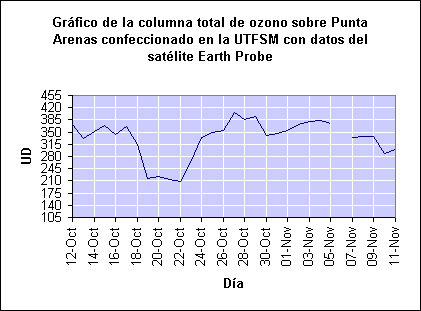
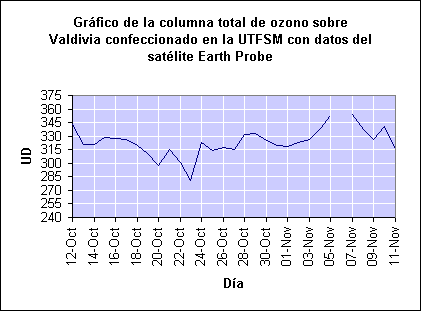
Para detectar si el agujero se extiende hasta el continente hay que definir primero cuánto ozono (medido en Unidades Dobson) se considera como un agujero. Es comunmente aceptado para el continente Sudamericano considerar una columna de ozono inferior a 220 UD para tal efecto. Ahora bien, estos niveles se han registrado algunos días del año en el extremo sur de Chile, como por ejemplo en Punta Arenas. Esto se produce en la "temporada", entre septiembre y noviembre, cuando se crea el agujero en la Antártica.



Según Sergio Cabrera, experto en ozono de la U de Chile, debido a importantes acuerdos sobre los usos de CFC y su notable disminución es de esperar que antes del 2050 el ozono se haya recuperado, ya que la curva de su deterioro ya comenzó a disminuír.
La Radiación Ultravioleta
La radiación ultravioleta está estrechamente ligada con el espesor de la capa de ozono, en especial la radiación UV-B. El siguiente esquema muestra el ancho de cada banda de UV-A, UV-B y UV-C.
Está claramente demostrado que mientras menor sea el espesor de la capa de ozono, mayor será la radiación UV. Esta radiación es útil para la fotosíntesis y también para fijar la vitamina D. Basta exponer la piel de 5 a 10 minutos al sol para que se fije la vitamina D. Eso sí, en exceso esta energética radiación quema las plantas y puede crear cáncer.
Repuesta de la piel
La respuesta de la piel se refiere a la manera en que la piel responde o reacciona frente a diferentes longitudes de onda, la cual no es lineal. Es decir, no toda longitud de onda afecta a la piel de la misma forma. Esto se hace evidente al observar que la luz
visible y el infrarojo no afectan a la piel, pero si nos afecta la radiación UV. También longitudes muy cortas y energéticas tampoco afectan en mayor medida a la piel. El siguiente gráfico se puede apreciar la respuesta de la piel a diferentes longitudes
de onda.
Daños que se pueden prever
1. Inicia y promueve el cáncer a la piel maligno y no maligno.
2. Daña el sistema inmunológico, exponiendo a la persona a la acción de varias bacterias y virus.
3. Provoca daño a los ojos, incluyendo cataratas.
4. Hace más severas las quemaduras del sol y avejentan la piel.
5. Aumenta el riesgo de dermatitis alérgica y tóxica.
6. Activa ciertas enfermedades por bacterias y virus.
7. Aumentan los costos de salud.
8. Impacta principalmente a la población indígena.
9. Reduce el rendimiento de las cosechas.
10. Reduce el rendimiento de la industria pesquera.
11. Daña materiales y equipamiento que están al aire libre.
Fuente: Universidad Federico Santa María, Chile